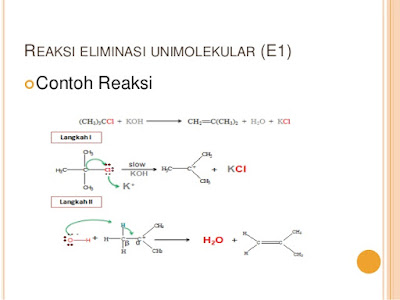
MEKANISME REAKSI ELIMINASI E1
MEKANISME REAKSI
ELIMINASI E1
Jika artikel sebelumnya, pembahasan
kita mengenai reaksi eliminasi E2. Selanjutnya pembahasan kita mengenai reaksi
eliminasi E1.
Ada
beberapa hal yang membedakan antara reaksi eliminasi E1 dengan E2, terutama
dari mekanismenya. Sebelumnya jika reaksi eliminasi E2 terjadi dengan satu
tahap dan secara serempak, maka pada reaksi eliminasi E1 ini terjadi secara dua
tahap.
Dan juga reaksi eliminasi juga
memakai dua komponen substituen sehingga dikenal juga dengan istilah reaksi
unimolekuler. Dan juga reaksi E1 ini juga melibatkan kehadiran karbokation
seperti pada reaksi Sn1.
Mekanisme reaksi E1 ini karena
adanya kehadiran karbokation, menjadikan mekanisme ini memiliki dua tahap. Yaitu
tahap satunya adalah pembentukan karbokation atau dengan istilah ionisasi. dan
tahap satunya lagi yaitu diprotonasi untuk menghilangkan ion yang berada pada
molekul karbokation tersebut.
PERMASALAHAN
11. Apa faktor pendukung terjadinya reaksi E1 ini?
22. Kenapa bisa terjadinya karbokation pada reaksi
E1 ini?
33. Apa yang membedakan reaksi E1 dan Sn1?
Saya ira desmila nim A1C117010 akan mencoba menjawab pertanyaan no 2 dari saudara habib, karbokation pada reaksi eliminasi dapat terbentuk dikarenakan terjadinya pemutusan atau lepas nya gugus pergi pada reaksi itu sendiri sehingga dapat terdorong dan mengakibatkan pembentukan karbokation, kemudian karbokation pada reaksi eliminasi E1 dapat terbentuk dikarenakan adanya ruang yang menyebabkan pembentukan karbokation itu sendiri, dan juga dikarenakan suasana polar pada reaksi E1 yang menyebabkan terbentuknya karbokation. Jadi itulah sebabnya mengapa karbokation dapat terbentuk.
BalasHapusSaya disa ananda nim A1C117072 kan membantu menjawab pertanyaan no 3
BalasHapusJelas berbeda dari namanya saja terdapat perbedaan yaitu substitusi dan eliminasi yang mengandung arti yang berbeda,tapi banyak juga kesamaan dalam reaksinya diantaranya
Pada sn1 :
-proses melalui 2 tahap
- Bereaksi dengan nukleofil lamah/basa lewis, ex: H2O, ROH
- Bereaksi baik dengan alkil
Tersier > sekunder (lambat)
- Pelarut polar
Sedangkan pada reaksi E1
Bereaksi dengan basa Bronsted Lowry lemah
Ex: H2O, ROH
- Bereaksi baik dengan alkil halida tersier > sekunder > primer
- Reaksi 2 tahap
- Pelarut polar protic
Saya Ariyansyah
BalasHapusNIM A1C117050
Saya akan mencoba membantu permasalahan no 1
Apa faktor pendukung terjadinya reaksi E1 ini?
Reaksi E1 terjadi karena adanya karbokation, jika karbokation ini tidak ada maka tidak terjadi reaksi ini.